服務熱線
86-21-54488867 / 4008202557
GB/T 15072.6-2025 貴金屬合金化學分析方法 第6部分:銥含量的測定
范圍
本文件描述了硫酸亞鐵電位滴定法測定貴金屬合金中銥含量的測定方法。
本文件適用于貴金屬合金中銥含量的測定。測定范圍(質量分數):5.00%~30.00%。
術語和定義
本文件沒有需要界定的術語和定義。
原理
試料置于聚四氟乙烯消化罐中,加鹽酸與H2O2,于烘箱中加熱溶解。釕元素用溴酸鈉氧化釕與基體分離,鈀元素用銅粉還原鈀與基體分離。在鹽酸和硫酸介質中,用硫酸亞鐵標準滴定溶液滴定將Ir(Ⅳ)還原至Ir(Ⅲ),電位法指示終點以測定銥含量。
試劑和材料
除非另有說明,在分析中僅使用確認為分析純的試劑和蒸餾水或去離子水或相當純度的水。
KClO3固體(優級純)。
銅粉:稱取1.0g鋅粉于100mL燒杯中,加1mL~2mL水潤濕。加10mL硫酸銅溶液(197g/L),搖動2min~3min,加30mL鹽酸。當劇烈反應停止后,傾潷上層溶液,加40mL鹽酸浸泡1h。傾潷上層溶液,用水清洗4次,倒去上層溶液。所得的活性銅粉供還原1份溶液使用。用時現配。
鹽酸(ρ=1.19g/mL)。
H2O2(ρ=1.10g/mL)。
硫酸溶液(1+1)。
硫酸溶液(4+96)。
氯化鈉飽和溶液。
氯酸鈉溶液(100g/L)。
溴化鈉溶液(100g/L)。
硫酸亞鐵標準滴定溶液[c(FeSO4•7H2O)約0.0011mol/L],按以下步驟配制和標定:
a) 配制:稱取0.318g硫酸亞鐵,溶入1000mL硫酸溶液中,混勻。
b) 標定:標定與試料的測定平行進行。移取10.00mL銥標準溶液3份,分別置于3個100mL高型燒杯中,各加入1滴氯酸鈉溶液,5mL鹽酸,混勻,靜置約10min。加入0.5mL氯化鈉飽和溶液、5mL硫酸溶液,加水至總體積約30mL。插入吹氣管,于吹氣裝置上吹氣10min,取下,用約10mL水沖洗吹氣管和高型燒杯壁,再重復吹氣10min。
將溶液轉入120mL滴定杯中。
將滴定杯放在滴定轉盤上,啟動自動電位滴定儀,將已連接在自動電位滴定儀上的電極和滴定管插入樣品溶液中,攪拌至少20s(設備參考參數見附錄A)。用硫酸亞鐵標準滴定溶液進行電位滴定至終點。從電位滴定曲線或dE/dV 曲線確定終點。記錄終點所消耗的硫酸亞鐵標準溶液體積V2。
平行標定3份,其標定所消耗硫酸亞鐵標準滴定溶液體積的極差值應不超過0.05mL,取其平均值。
按公式(1)計算硫酸亞鐵標準滴定溶液的實際濃度:![]()
式中:
c ——硫酸亞鐵標準滴定溶液的實際濃度,單位為摩爾每毫升(mol/mL);
ρ0——銥標準溶液的質量濃度,單位為毫克每毫升(mg/mL);
V1——移取銥標準溶液的體積,單位為毫升(mL);
192.22——銥的摩爾質量,單位為克每摩爾(g/mol);
V2——標定時,滴定銥標準溶液所消耗硫酸亞鐵標準滴定溶液的體積,單位為毫升(mL)。
銥標準溶液:稱取0.10g銥粉(ωIr≥99.99%),精確至0.00001g,于50mL硬質玻璃封管,加入10mL鹽酸,700mg KClO3置于氣體反應支架內,氣體反應支架置于硬質玻璃封管中,于300°C溶解至少6h。將管內試液移入200mL容量瓶中,用水沖洗4次~5次,加入100mL鹽酸,用水稀釋至刻度。混勻。此溶液1mL含0.5mg銥。
儀器設備
天平:感量0.01mg。
滴定裝置:自動電位滴定儀。儀器工作參考參數見附錄A。
聚四氟乙烯消化罐: 壁厚25mm±2mm,容積30mL,達到以上條件的消化罐均可使用。
烘箱(溫度不大于300°C)。
恒溫磁力攪拌器。
吹氣裝置,如圖1所示。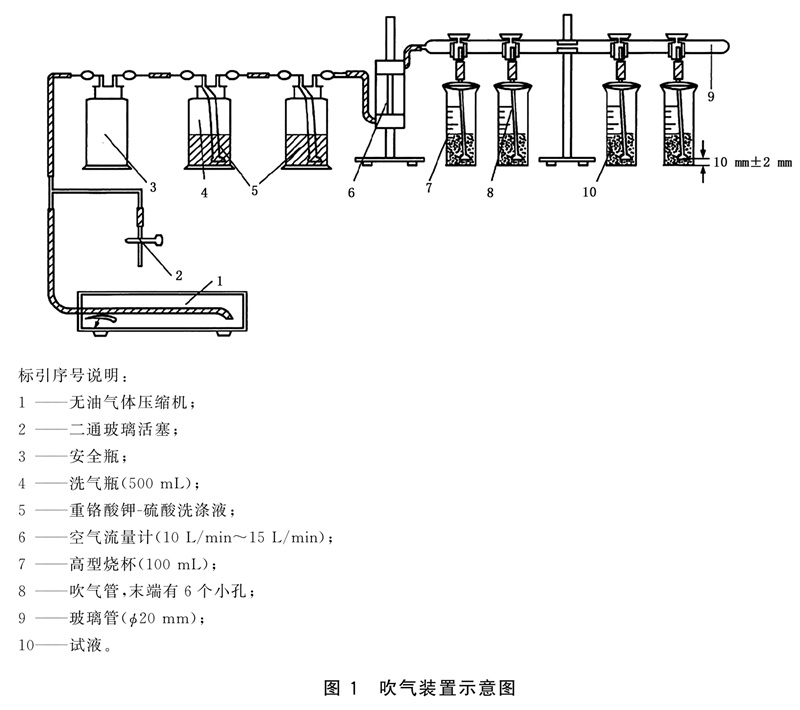
樣品
樣品加工成碎屑,碎屑的厚度不大于0.2mm,長度、寬度不大于2.0mm。用冰醋酸浸泡10min后,再用無水乙醇洗凈、晾干,混勻。
試驗步驟
試料
稱取0.1g樣品,精確至0.00001g。
平行試驗
平行做兩份試驗,取其平均值。
空白試驗
隨同試料做空白試驗。
測定
試樣溶解
將試料置于聚四氟乙烯消化罐中,加20mL鹽酸、5mL H2O2,密封聚四氟乙烯消化罐,于烘箱中150°C±5°C溶解36h。待冷卻至室溫,銥含量不大于10%的試液轉入50mL容量瓶中,銥含量>10%的試液轉入100mL容量瓶中,以水稀釋至刻度,混勻。
試液的處理
不含釕和鈀試液的處理
移取20mL試液于100mL高型燒杯中,加入5mL鹽酸、5mL硫酸溶液、0.5mL氯化鈉飽和溶液。
含釕試液的處理
移取20mL試液于100mL燒杯,加0.5mL氯化鈉飽和溶液,蒸至濕鹽狀。加入約1mL水,再次蒸至濕鹽狀,反復2次。加入0.5mL溴酸鈉溶液蒸至近干,重復3次。加入5mL鹽酸將沉淀溶解,沖洗表面皿和杯壁,將溶液濃縮至體積約1mL,將溶液轉入聚四氟乙烯消化罐中,加7mL鹽酸、1.5mL H2O2,密閉聚四氟乙烯消化罐,置于烘箱中150°C±5°C溶解6h。取出,冷卻至室溫,將試液轉入100mL高型燒杯中,加入5mL鹽酸、5mL硫酸溶液。
含鈀試液的處理
移取20mL試液于100mL燒杯中,置于電爐上,低溫蒸發至2mL,取下。加40mL鹽酸和銅粉,將燒杯放入恒溫磁力攪拌器上的水浴皿中,在50°C~60°C 的水浴中加熱攪拌30min,取下。用中性濾紙過濾,濾液濾入200mL燒杯中,用鹽酸洗滌燒杯及沉淀4次~5次,棄去沉淀。濾液于電爐上低溫蒸發至5mL,加入10mL鹽酸、2mL氯酸鈉溶液,蓋上表面皿,再煮沸至5mL,取下。試液轉入100mL 高型燒杯中,用鹽酸洗滌燒杯壁和表面皿,每次2mL,再用水沖洗4次,每次約2.5mL。加1mL氯酸鈉溶液,混勻。靜置10min,加入20mL硫酸溶液。
含釕和鈀試液的處理
移取20mL試液于100mL燒杯,加0.5mL氯化鈉飽和溶液,蒸至濕鹽狀。加入約1mL水,再次蒸至濕鹽狀,反復2次。加入0.5mL溴酸鈉溶液蒸至近干,重復3次。加入5mL鹽酸將沉淀溶解,沖洗表面皿和杯壁,將溶液濃縮至體積約2mL,取下。加40mL鹽酸和銅粉,將燒杯放入恒溫磁力攪拌器上面的水浴皿中,在50°C~60°C的水浴中加熱攪拌30min,取下。用中性濾紙過濾,濾液濾入200mL燒杯中,用鹽酸洗滌燒杯及沉淀4次~5次,棄去沉淀。
濾液于電爐上低溫蒸發至1mL,將溶液轉入聚四氟乙烯消化罐中,加7mL鹽酸、1.5mL H2O2,密閉聚四氟乙烯消化罐,置于烘箱中150°C±5°C溶解6h。取出,冷卻至室溫,將試液轉入100mL高型燒杯中,加入5mL鹽酸、5mL硫酸溶液。
吹氣
于試液中,插入吹氣管,在吹氣裝置上吹氣。先吹氣10min,用約10mL水沖洗高型燒杯壁和吹氣管,再吹氣10min,取下。用約5mL水沖洗吹氣管和高型燒杯,重復3次,將試液轉入120mL滴定杯中。
滴定
將滴定杯放在滴定轉盤上,啟動自動電位滴定儀,將已連接在自動電位滴定儀上的電極和滴定管插入樣品溶液中,攪拌至少20s(設備參考參數見附錄A),用硫酸亞鐵標準滴定溶液進行電位滴定至終點。從電位滴定曲線或dE/dV曲線確定終點。記錄終點所消耗的硫酸亞鐵標準滴定溶液體積。
試驗數據處理
銥含量以依的質量分數ωIr計,按公式(2)計算:![]()
式中:
c ——硫酸亞鐵標準滴定溶液的實際濃度,單位為摩爾每毫升(mol/mL);
V5——滴定試液所消耗的硫酸亞鐵標準滴定溶液的體積,單位為毫升(mL);
V0——滴定空白所消耗的硫酸亞鐵標準滴定溶液的體積,單位為毫升(mL);
V3——試液總體積,單位為毫升(mL);
192.22——銥的摩爾質量,單位為克每摩爾(g/mol);
m0——試料的質量,單位為克(g);
V4——分取試液體積,單位為毫升(mL)。
試驗結果的數值按 GB/T 8170 的規定進行修約,計算結果表示到小數點后兩位。
京都電子KEM 自動電位滴定儀 AT-710S